在肿瘤与自身免疫性疾病治疗领域,T 细胞衔接器(T-cell engagers, TCEs)作为一种创新性的双/多特异性抗体平台,正迅速成为免疫治疗的新基石。
本文将从研发背景、核心机制、临床进展与未来方向等多个维度,系统解析 TCEs 的技术突破与治疗前景。
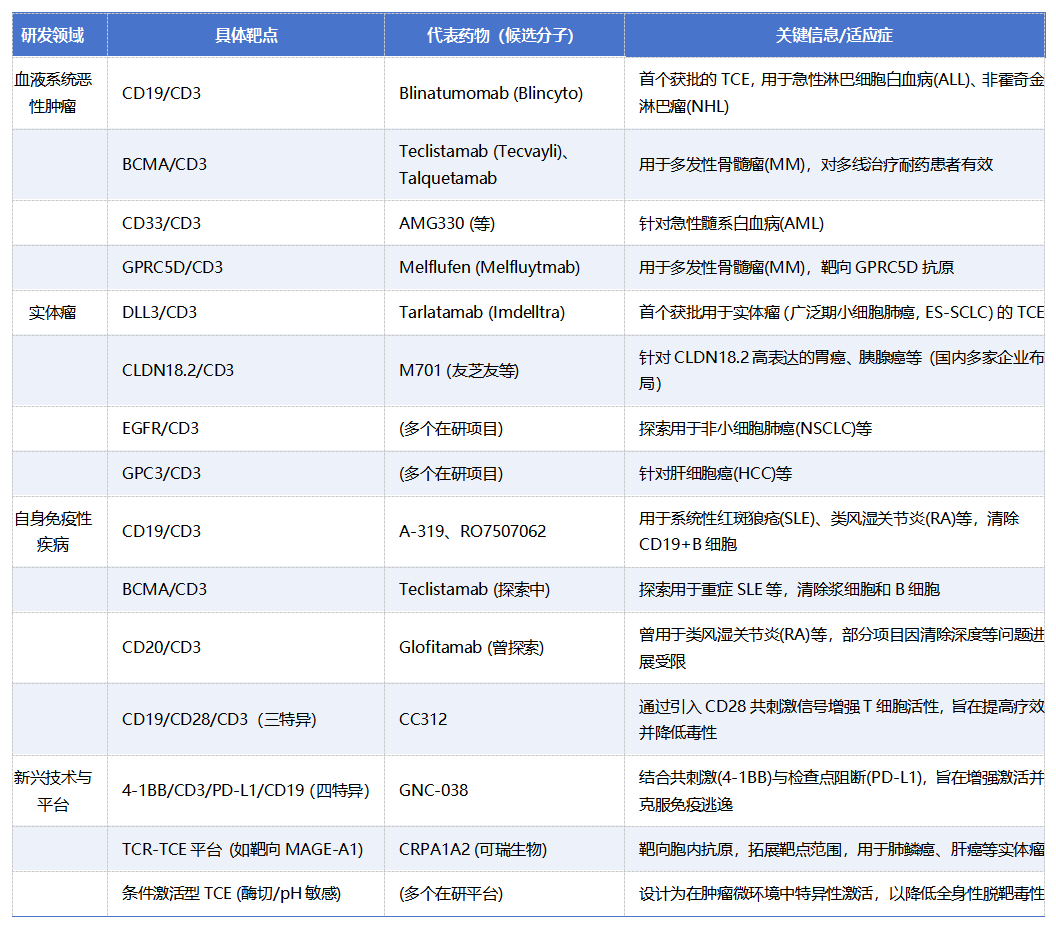
表:TCEs 管线信息 来源:丁香通
一、研发背景与核心机制
1. 研发背景
肿瘤免疫治疗领域的发展,遵循着从直接杀伤到调动内源性免疫、再到精准工程化免疫细胞的技术路径。
-
以化疗和靶向药物为代表的第一代疗法,虽能直接杀伤肿瘤细胞,但无法调动宿主免疫系统,且易产生耐药。
-
以 PD-1/PD-L1 抑制剂为代表的免疫检查点抑制剂(ICIs)能够解除 T 细胞的抑制状态,但其疗效高度依赖于肿瘤自身的免疫原性和预先存在的肿瘤浸润淋巴细胞,导致仅约 20-30% 的患者能够持久获益。
-
以 CAR-T 为代表的过继性细胞疗法在血液系统肿瘤中展现出革命性疗效,但在实体瘤中面临浸润困难、靶点异质性及安全性挑战,且存在生产成本高、制备周期长等问题。
在此背景下,T 细胞衔接器(TCEs)应运而生。它兼具抗体的靶向性与 T 细胞激活能力,为肿瘤治疗提供了新的策略。
与此同时,在自身免疫性疾病领域,传统糖皮质激素与广谱免疫抑制剂往往仅能控制症状,且伴随长期副作用与高复发率。TCEs 在这一领域的应用逻辑与之呼应:通过靶向致病性免疫细胞(如 B 细胞、浆细胞或异常 T 细胞)表面特定抗原(如 CD19、BCMA、CD38),并借助 CD3 重定向内源性 T 细胞,从而精准清除致病细胞群,实现从「广泛免疫抑制」到「精准免疫调节」的治疗模式转变。这既延续了 TCEs 在肿瘤治疗中的核心机制,也为其在自免疾病中的创新应用奠定了理论基础。
2. TCE 的定义与机制突破
TCEs 是一类工程化的双特异性或多特异性抗体分子。其核心机制在于,通过单一分子桥接 T 细胞与靶细胞:一端(通常为低亲和力)结合 T 细胞表面的 CD3ε 链,另一端(通常为高亲和力)结合靶细胞(肿瘤细胞或异常免疫细胞)表面的特异性抗原。
这种物理连接在两者之间直接形成「免疫突触」,绕过了传统 T 细胞激活所必需的 MHC-抗原呈递过程。连接一旦建立,便会强力激活 T 细胞,导致其释放穿孔素、颗粒酶等细胞毒性物质,并上调凋亡配体表达,从而直接诱导靶细胞凋亡。
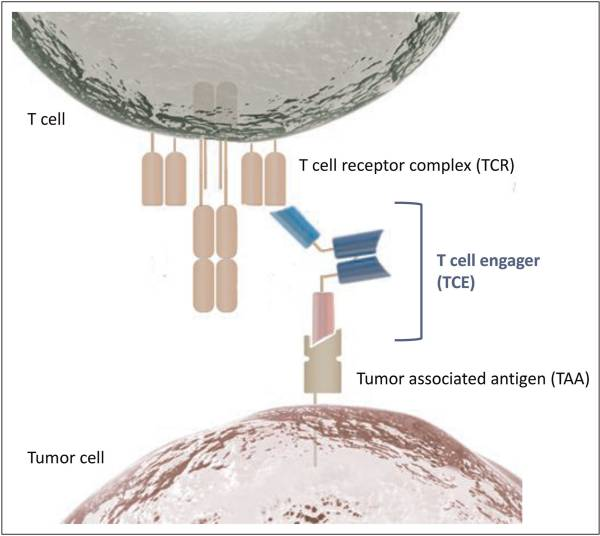
TCE 机制图
核心机制突破:
与传统免疫检查点抑制剂仅「解除 T 细胞抑制」的被动机制不同,TCEs 通过其结构实现了「主动重定向与直接激活」。该机制不依赖于 MHC 介导的抗原呈递,可直接将 T 细胞杀伤活性导向特定靶细胞,从而克服了免疫检查点抑制剂(ICI)疗法 对肿瘤免疫原性的依赖。
二、TCEs 在免疫治疗中的突破性应用
1. 突破 PD-1/PD-L1 抑制剂的疗效局限
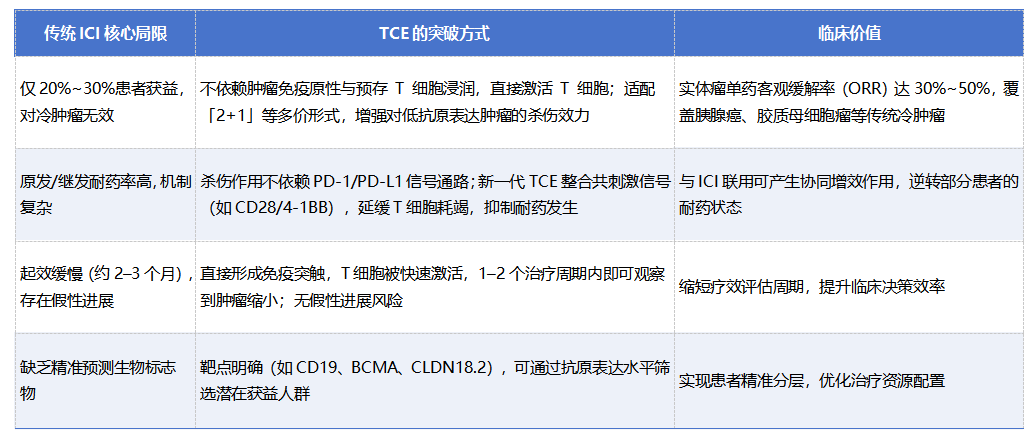
2. 弥补 CAR-T 疗法的临床应用短板

3. 优化自身免疫疾病治疗的精准性与安全性
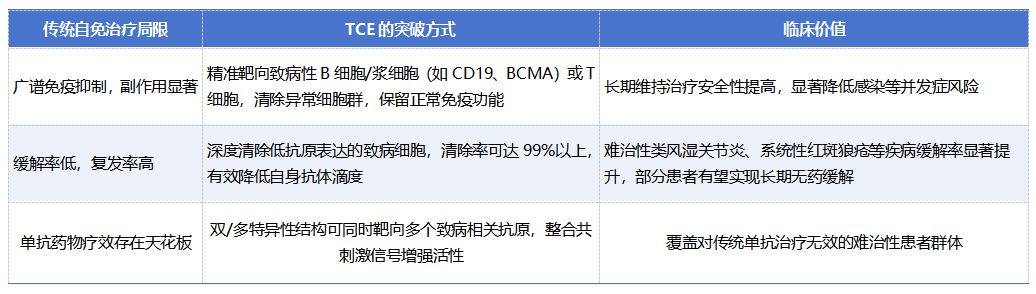
4. TCE 与 ADC 疗法的核心差异与协同潜力
抗体药物偶联物(ADC)通过靶向递送细胞毒性药物杀伤肿瘤细胞,而 TCEs 则通过桥接 T 细胞实现免疫介导的杀伤,二者在机制与特征上存在系统性差异。TCE 与 ADC 的联合应用已成为临床研究的重要方向,其原理在于:ADC 杀伤高抗原表达的肿瘤细胞后释放肿瘤抗原,可进一步增强 TCE 的免疫激活效果,形成「靶向杀伤+免疫清除」的协同效应,有望显著提升客观缓解率并延长生存期。

表:TCE 与 ADC 疗法对比
值得一提的是,TCE 与 ADC 的联合应用已成为临床研究的重要方向,其原理在于:ADC 杀伤高抗原表达的肿瘤细胞后释放肿瘤抗原,可进一步增强 TCE 的免疫激活效果,形成「靶向杀伤+免疫清除」的协同效应,有望显著提升客观缓解率并延长生存期。
三、TCEs 的临床应用进展与核心挑战
1. 临床应用进展
TCEs 的临床应用已形成从血液瘤向实体瘤拓展,并在自身免疫性疾病领域实现初步探索的格局。
当前研究主要聚焦于疗效提升、毒性控制与应用范围拓展三大方向。
肿瘤治疗领域
血液瘤:已成为复发/难治性血液瘤的核心治疗选择。代表性药物包括:
-
Blinatumomab(CD19/CD3 双抗):全球首款获批 TCE,用于 B-ALL,完全缓解率(CR)达 40%-50%,显著优于传统化疗。
-
Teclistamab(BCMA/CD3 双抗):用于多发性骨髓瘤,单药 ORR 超过 60%,对 CAR-T 治疗失败的患者仍具疗效。
-
Epcoritamab(CD20/CD3 双抗):采用皮下注射,ORR 达 70% 以上,安全性良好。
实体瘤:近期取得关键突破。
-
靶向 DLL3 的 Tarlatamab 获批用于小细胞肺癌,ORR 为 20%-30%,打破了实体瘤 TCE 治疗的僵局。
-
针对 CLDN18.2、PSMA、EGFR 等靶点的 TCEs 已进入临床Ⅱ期。例如,CLDN18.2/CD3 双抗在晚期胃癌中 ORR 达 35%-45%。
-
联合策略:与细胞因子药物(如长效 IL-7)联用,可显著增强实体瘤中 T 细胞的数量与功能,提升疗效。
-
前沿技术:mRNA 编码 TCE 技术取得进展,如 MTS-105 通过 LNP 靶向递送,在肝细胞癌模型中实现肿瘤完全消退并诱导免疫记忆。
自身免疫性疾病领域
-
临床探索:目前处于早期阶段,但初步数据展现出潜力。例如,在难治性 SLE 和 RA 中,CD19/CD3 双抗可实现深度 B 细胞清除,疾病缓解率显著提高。
-
技术优化:通过低亲和力 CD3 结合域与 Fc 段沉默设计,降低 CRS 风险,适配长期管理需求。
2. 核心挑战
毒性控制:
-
CRS 与 ICANS 是主要剂量限制性毒性。
应对策略包括低亲和力 CD3 设计、条件激活型前药(Pro-TCE)以及预防性用药。
耐药机制:
-
靶点下调或丢失;
-
T 细胞功能耗竭。
应对方向:开发多靶点 TCEs、整合共刺激信号、与免疫调节药物联用。
适应症拓展:
探索在罕见血液瘤、儿科肿瘤及特定难治性自身免疫疾病中的应用。
四、未来发展方向
-
多特异性平台拓展:开发三/四特异性 TCEs,整合共刺激/共抑制信号,提升特异性与活性 3,4。
-
新型递送技术:mRNA-TCE 等平台技术有望实现体内原位表达,优化药物分布。
-
靶点范围突破:基于 TCR 的 TCEs 可靶向细胞内抗原,极大扩展靶点空间。
-
自身免疫疾病治疗深化:推动从「症状控制」向「病因干预」的治疗目标转变。
五、总结
TCEs 通过其「主动重定向」的核心机制,在肿瘤与自身免疫性疾病治疗中展现出突破性潜力。其「现货型」、高活性与可工程化优化的特性,正在重塑免疫治疗的研发格局与临床实践。未来,随着多特异性设计、联合策略优化与新型技术平台的成熟,TCEs 有望成为跨越多种疾病类型的基石性疗法。
来源:丁香通
参考文献:
1.Baeuerle, P.A. and H. Wesche, T-cell-engaging antibodies for the treatment of solid tumors: challenges and opportunities. Curr Opin Oncol, 34(5): p. 552-558.
2.Dicara, D.M., et al., Development of T-cell engagers selective for cells co-expressing two antigens. MAbs, 14(1): p. 2115213.
3.Zarezadeh Mehrabadi, A., et al., Revolutionizing cancer treatment: the power of bi- and tri-specific T-cell engagers in oncolytic virotherapy. Front Immunol, 15: p. 1343378.
4.Park, D.H., et al., Novel tri-specific T-cell engager targeting IL-13Rα2 and EGFRvIII provides long-term survival in heterogeneous GBM challenge and promotes antitumor cytotoxicity with patient immune





