在全球,结直肠癌是发病率第三、死亡率第二的恶性肿瘤。
临床最残酷的现实是:约 30%~40% 患者会发生肝转移,肝脏是第一致命转移部位。
更无奈的是:免疫治疗来了,但结直肠癌肝转移(CRLM)对 PD1 普遍耐药,疗效大打折扣。
为什么肝转移灶如此 “顽固”?谁在保护肿瘤、抵抗免疫、驱动扩散?
近日,北京大学肿瘤医院团队在Cancer Research(IF=13.3)上发表题为“SPP1 Drives Colorectal Cancer Liver Metastasis and Immunotherapy Resistance by Stimulating CXCL12 Production in Cancer-Associated Fibroblasts”的研究成果。用空间转录组、单细胞测序、类器官、人源化模型,首次完整揭示:SPP1-CAF-CXCL12 轴是结直肠癌肝转移与免疫耐药的核心元凶!
·核心机制·
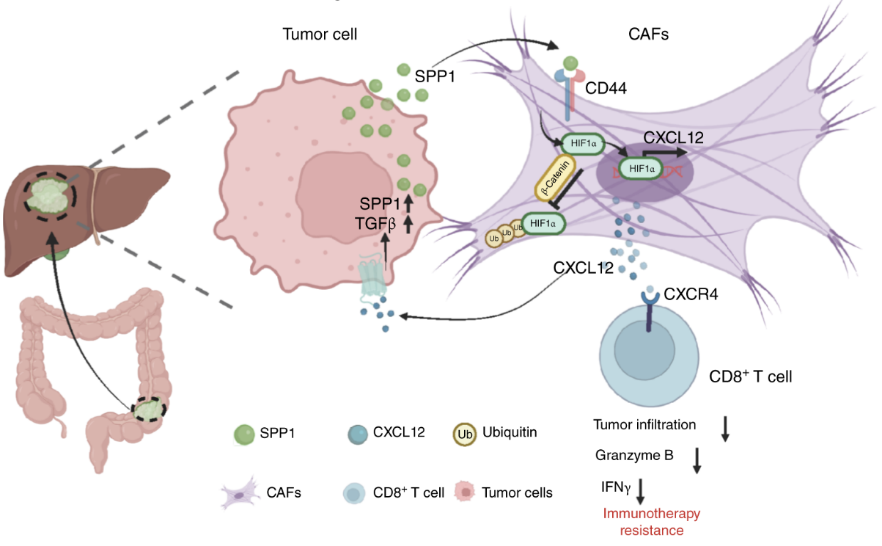
CRC 肿瘤细胞高分泌SPP1→结合 CAFs 的CD44→激活βcatenin/HIF1α→CAFs 大量分泌CXCL12
🔷 正向:促进 CRC 细胞 EMT 与转移,上调 SPP1 形成正反馈
🔷 负向:抑制 CD8+T 细胞浸润与毒性→肝转移 + 免疫治疗耐药
·创新与亮点·
🔷 新机制:首次完整解析SPP1/βcatenin/HIF1α/CXCL12轴驱动 CRLM 与免疫逃逸的完整通路。
🔷 新靶点:证实SPP1 与 CXCL12是双靶点,联合免疫检查点抑制剂具有治疗潜力。
🔷 新标志物:血浆 SPP1可无创预测 CRLM 免疫治疗疗效,便于临床转化。
临床导向:从临床问题出发,干湿结合,覆盖细胞-动物-患者全链条验证。
·研究结果·
1. SPP1 在 CRLM 中显著上调,与肝转移及免疫耐药正相关
🔷 多个bulk RNA-seq数据集:联合锁定SPP1为 CRLM 共同上调基因。
🔷 临床样本:肝转移灶 SPP1 表达、血浆 SPP1 水平显著高于原发灶;高 SPP1 提示转移、预后差、免疫治疗不响应。利用来自结直肠癌患者原发肿瘤组织的空间转录组数据,研究了SPP1在CRLM免疫治疗耐药中的作用。簇1主要与残余肿瘤区域相关,表现出显著的SPP1富集。
🔷 细胞/动物:过表达 SPP1 增强迁移、侵袭与肝转移能力。
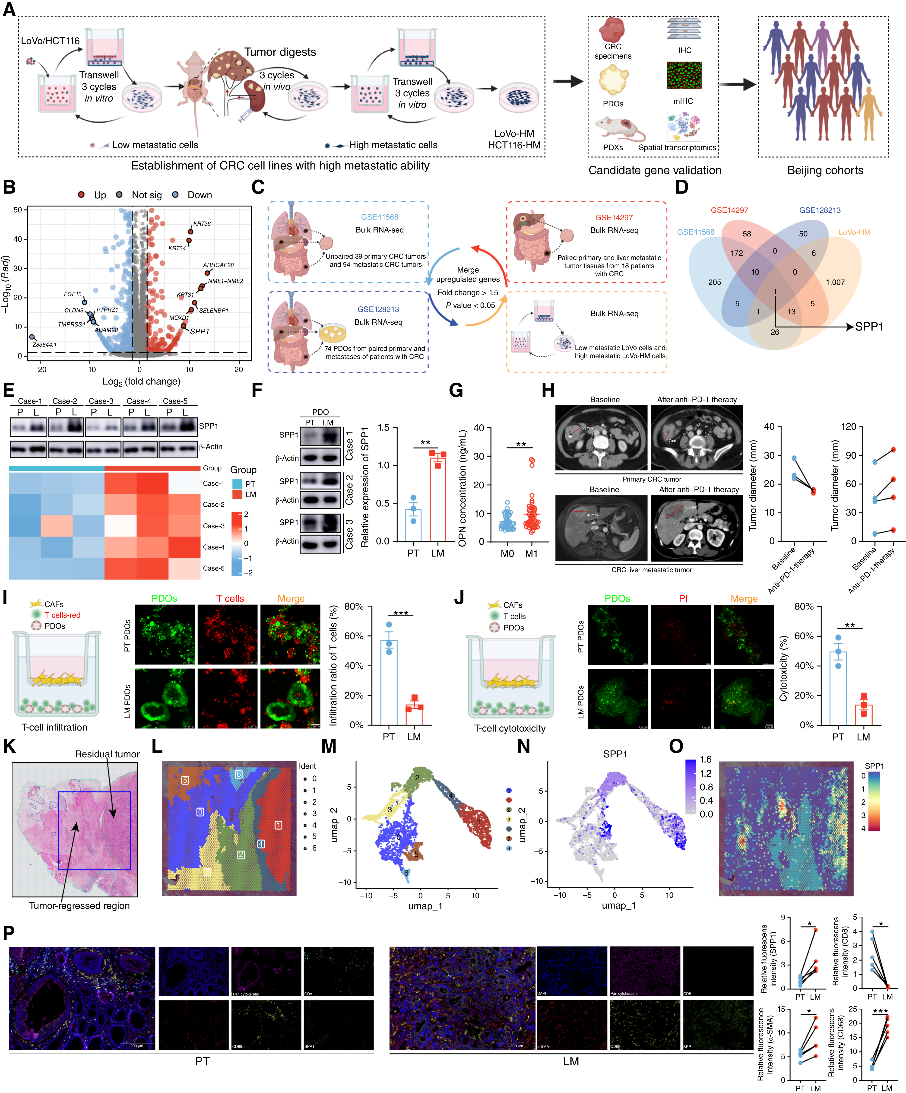
图1 SPP1 高表达与结直肠癌肝转移 (CRLM) 和免疫治疗耐药相关
2. SPP1 通过招募并激活 CAFs,重塑促瘤微环境
🔷 SPP1 与 CAFs 浸润、活化标志物(αSMA、FAP)正相关。通过对MC38异种移植瘤进行单细胞RNA测序,进一步验证了SPP1对不同TME细胞群的影响,发现SPP1过表达后成纤维细胞数量增加,而T细胞数量相应减少。
🔷 SPP1 直接促进 CAFs 迁移、增殖、胶原收缩,增强 CAFs 的恶性表型。
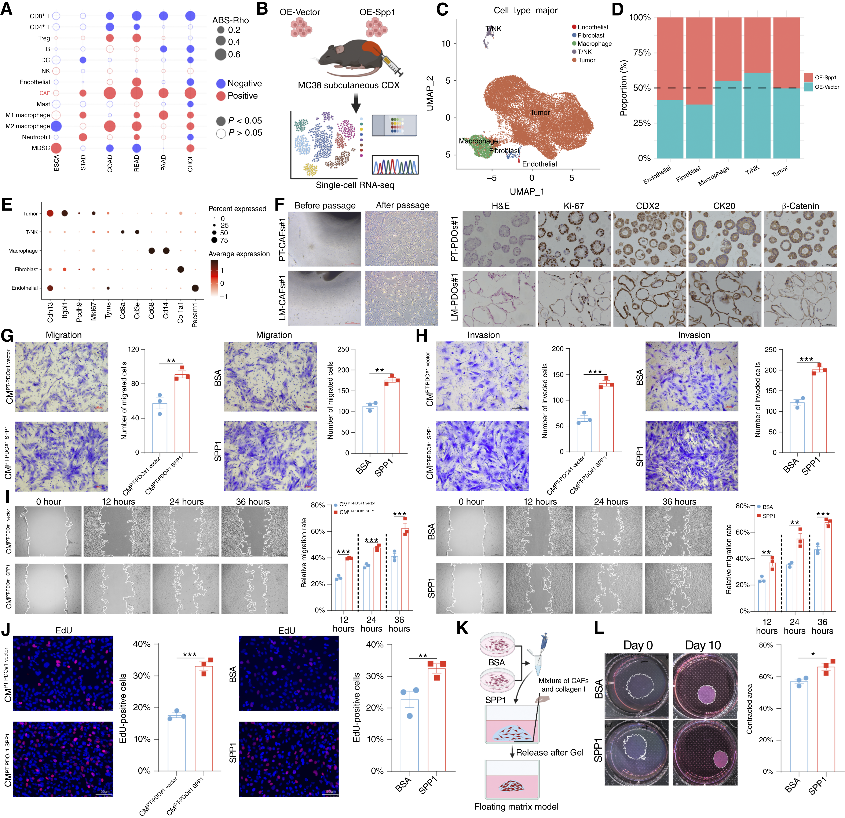
图2 SPP1增强CAFs向TME的浸润并促进其恶性表型
3. CXCL12 形成正反馈,驱动转移并抑制免疫
🔷 促转移:CXCL12 促进 CRC 细胞EMT、迁移、侵袭,并上调 SPP1/TGFβ,形成SPP1CAFCXCL12 正反馈环。对先前获得的MC38异种移植瘤单细胞测序数据重新分析表明,Spp1过表达显著增加了表达CXCL12的CAFs谱系。
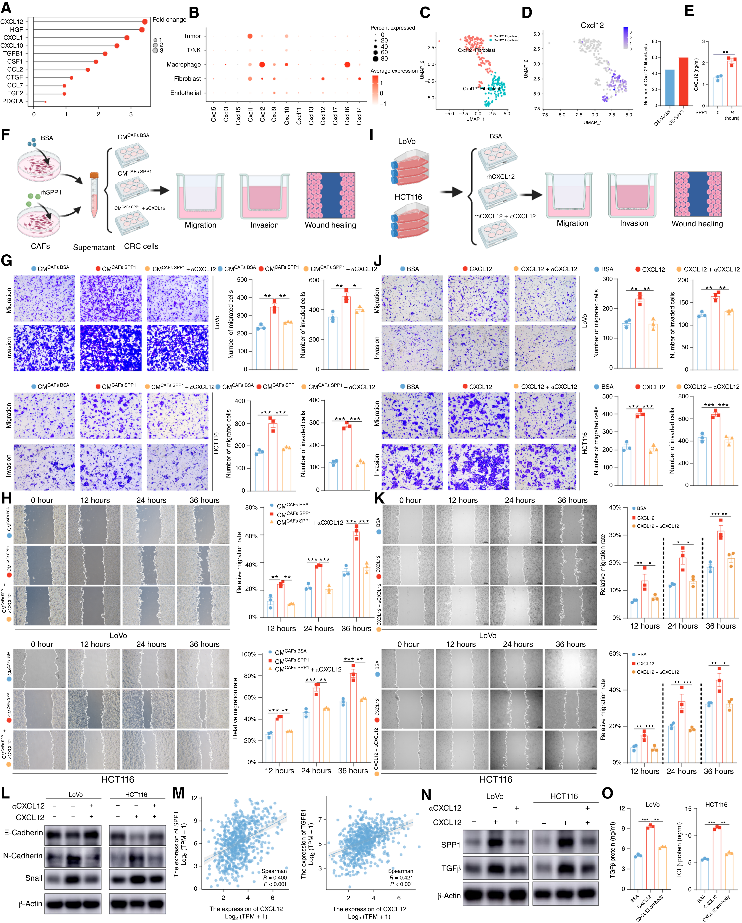
图3 SPP1通过CAF分泌的CXCL12介导的正反馈回路促进结直肠癌转移
🔷 免疫抑制:肿瘤细胞衍生的 SPP1 通过增强 CAFs 分泌 CXCL12 来抑制CD8+T细胞浸润和细胞毒性。
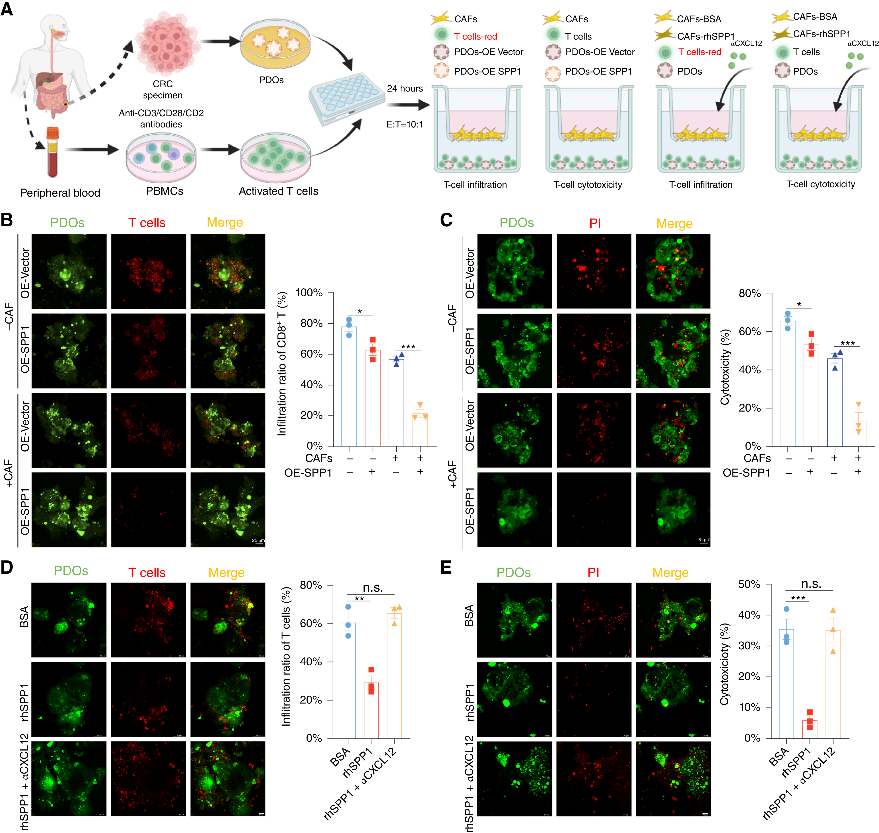
图4 SPP1通过抑制CAFs分泌CXCL12来抑制T细胞浸润和细胞毒性
4. SPP1激活CAFs中的β-catenin/HIF1α轴,从而驱动CXCL12分泌
🔷 SPP1 结合 CAFs 表面CD44受体。
🔷 激活βcatenin/HIF1α通路,βcatenin 稳定 HIF1α 蛋白并促核转位。
🔷 HIF1α 结合 CXCL12 启动子HBS1 位点,直接转录上调CXCL12分泌。
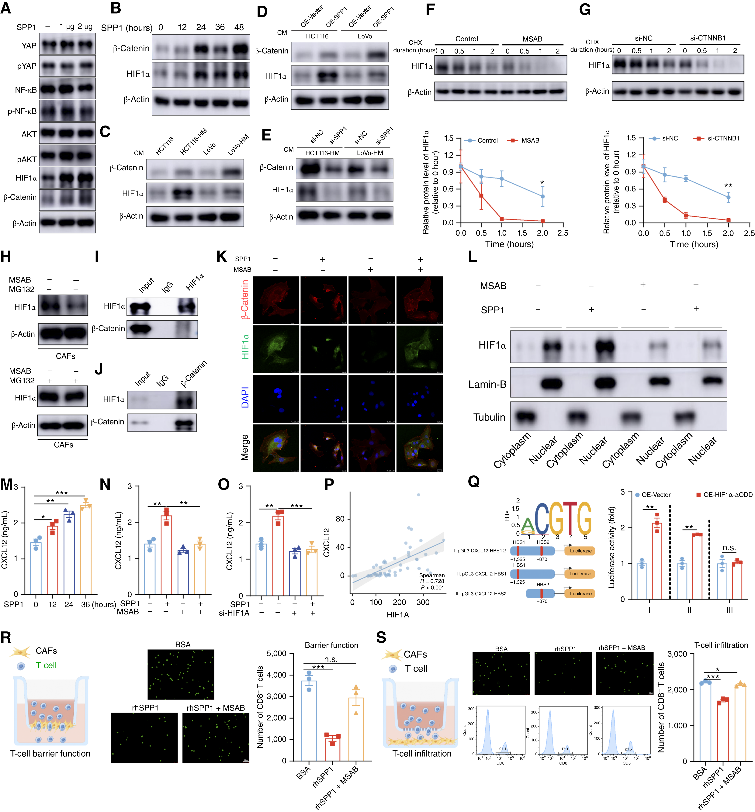
图5 SPP1激活CAFs中的β-catenin/HIF1α轴,从而驱动CXCL12的分泌
5. 靶向 SPP1/CXCL12 轴逆转免疫耐药,协同抗 PD1
🔷 干预方式:抗 SPP1 抗体、CXCR4 拮抗剂(Plerixafor)、CAF 抑制剂(Talabostat)。
🔷 效果:抑制肝转移、降低 CAF 活化、恢复 CD8+T 浸润,与抗 PD1协同增效。
🔷 临床转化:血浆 SPP1/CXCL12 可预测免疫治疗响应,高表达者更易耐药。
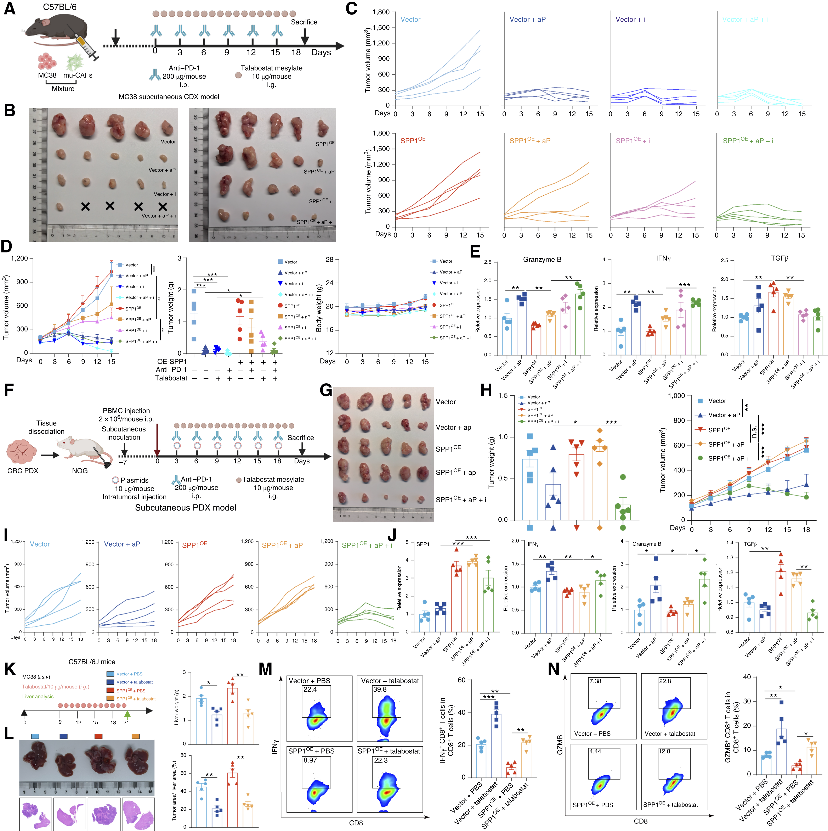
图6 Talabostat可逆转结直肠癌肝转移进展,并与PD-1阻断疗法产生协同作用





